骨芽細胞腫
記事の医療専門家
最後に見直したもの: 29.06.2025
骨芽細胞腫は、良性または悪性の腫瘍であり、様々な骨格骨に損傷を与えます。当初、この病理は巨大細胞腫瘍(1912年以降)と呼ばれていましたが、10年後、スチュワート博士が骨芽細胞腫という名称を提案しました。そして1924年になってようやく、ルサコフ教授が腫瘍の細胞構成をより正確に反映した「骨芽細胞腫」という明確な用語を導入しました。
今日では、骨芽細胞腫は真の腫瘍、すなわち広範な血管網を有する軟部組織腫瘍とみなされています。唯一の適切な治療法は、健常組織内で腫瘍を切除することであり、場合によっては骨移植も同時に行われます。[ 1 ]
疫学
世界における骨腫瘍の発生率は0.5~2%です。米国の統計によると、骨肉腫(症例の約34%)、軟骨肉腫(27%)、ユーイング腫瘍(18~19%)が最も多く見られます。脊索腫、線維肉腫、線維肉腫、組織球腫、巨細胞腫、血管肉腫はそれほど多くありません。
発生率は年齢と高い相関関係にあります。そのため、腫瘍の成長の最初の急増は思春期(16歳前後)に見られ、2回目の急増は中年期に見られます。
骨芽細胞腫は比較的よく見られる腫瘍です。骨腫瘍全体の約2~30%を占めます。女性に多く見られますが、男性にも発症する可能性があり、主に18歳から40歳の間で発症します。12歳未満の小児に発症することは稀ですが、この年齢層でも発症の可能性は否定できません。骨芽細胞腫には、家族性および遺伝性の症例が報告されています。
ほとんどの場合(約 75%)、腫瘍は長い管状の骨に見つかりますが、扁平骨や小骨が影響を受けることはあまりありません。
長管骨では、主に骨幹端が侵され、小児期には骨幹端が侵されます。腫瘍は骨端線や関節軟骨の領域には広がりません。骨幹に問題が見つかることは非常に稀です(症例の0.5%未満)。
医学の発展に伴い、骨芽細胞腫の発生率は安定しているものの、死亡率は大幅に低下していることが指摘されています。病態の主因であり、最も可能性の高い原因は電離放射線の影響と考えられています。そのため、高線量放射線療法を受けた人や、診断または治療目的で放射性同位元素を注射された患者では、リスクが高まります。その他の一般的な病因としては、不適切な生態や遺伝などが挙げられます。[ 2 ]
原因 骨芽細胞腫
骨芽細胞腫は、病的に変化した細胞の集塊であり、骨格のほぼあらゆる部位に出現する可能性があります。構造異常にもかかわらず、病的な細胞は健常組織と同様に分裂を続けます。病的な細胞の構造は正常とは大きく異なり、直接影響を受けた骨の特性と通常の機能が置き換えられます。病的に変化した悪性細胞は、制御不能で、しばしば急速に増殖する傾向を獲得し、その結果、腫瘍の体積が増加します。以前は正常であった骨組織は腫瘍の構造によって置き換えられ、個々の病的な細胞は分離され、血液またはリンパ液によって他の遠隔解剖学的領域に輸送される可能性があります。このようにして転移が形成されます。
悪性骨芽細胞腫の発生源は、体内のあらゆる部位に存在するあらゆる悪性腫瘍(内臓腫瘍を含む)であることが知られています。その進行経路は転移です。しかし、ほとんどの骨芽細胞腫(良性、悪性ともに)は、最初に同じ部位に発生し、発達する原発性腫瘍です。
一般的に、骨芽細胞腫は多因子性腫瘍であり、その正確な原因は現時点では解明されていません。腫瘍の発生には以下のような条件が挙げられます。
- 免疫不全状態。
- 先天性組織の変化
- 変異誘発性の環境の影響
- ホルモンの変化;
- 同時発生している病状および傷害(病歴には外傷がしばしば記載されている)。
危険因子
骨芽細胞腫の形成原因に関する正確なデータは不足しています。しかし、専門家は、骨腫瘍のリスク増加に関連するいくつかの要因が関与していると示唆しています。
- 遺伝。多くの場合、腫瘍形成の傾向は遺伝的に決定されます。特に、癌性腫瘍や肉腫を含む様々な腫瘍の発生を促進するリー・フラウメニ症候群がこれに該当します。
- パジェット病。この病気は1つまたは複数の骨に影響を及ぼす可能性があり、腫瘍の前段階の病態に属します。この疾患の患者では、骨が肥厚すると同時に脆くなり、病的骨折が頻繁に起こります。重症パジェット病の症例の約8%に骨肉腫が発生します。
- 複数の骨の過成長、外骨腫。
- 多発性骨軟骨腫(遺伝性を含む)。
- 多発性軟骨腫(リスクは小さいですが、依然として存在します)。
- 放射線被曝(他の腫瘍過程の治療に使用される強力な放射線や、放射性ラジウムおよびストロンチウムの影響を含む)。
特別なリスクのカテゴリーには、60 グレイを超える線量を受ける小児期および若年期の放射線治療が含まれます。
専門家は、非電離放射線、特に電力線、携帯電話、家電製品から発生するマイクロ波や電磁放射線は骨芽細胞腫のリスクをもたらさないという事実に注目している。
病因
骨芽細胞腫の出現と発達の病態学的特徴は、病理の複雑さゆえに完全には解明されていません。腫瘍形成の根本的な原因は、免疫系の機能不全による細胞分化の失敗です。その結果、「誤った」未分化細胞からなる腫瘍が増殖し、腫瘍の特性を決定づけ、構造的には未熟細胞に類似します。細胞構造が正常に近いものの、正常と異なる場合は、良性の骨芽細胞腫と呼ばれます。細胞構造に顕著な変化が見られる場合は、悪性過程に起因すると考えられます。このような腫瘍では、抗原性細胞襞の変化、制御不能な増殖、細胞分裂が典型的に見られます。細胞構造の特異性の喪失に伴い、機能性も損なわれます。悪性骨芽細胞腫は、良性骨芽細胞腫とは異なり、周囲の健常組織への浸潤過程において他の腫瘍と大きく異なります。良性骨腫瘍では、健常組織への腫瘍の増殖は見られず、急速な増殖や全身への転移も見られず、腫瘍の分解産物による自己破壊や中毒も起こりません。
病状の良性・悪性に関わらず、いずれの症例でも骨構造は破壊されます。その結果、患部の骨は脆くなり、脆くなります。医師の診察を受ける理由の多くは、最小限の負荷でも発生する病的骨折です。
留意すべき重要な点は、プロセスの良性は常に条件付き状態であり、悪性化のリスクがあり、良性の病巣が変形すると悪性の骨芽細胞腫が発生する可能性があるためです。
症状 骨芽細胞腫
骨芽細胞腫の臨床像は、主に病変の局在と病期によって異なります。一般的に、腫瘍は以下の特徴を示します。
- 腫瘍は孤立性です。
- 主に下肢または上肢の管状骨に影響します。
- 扁平骨ではあまり見られません。
- 影響を受けた部分にしつこい痛みがあります。
- 病変部位の皮膚および血管のパターンが増加する。
- 患肢が変形する(局所的な体積増加)
- 骨芽細胞腫に最も近い関節または四肢全体の機能に障害が起こります。
- 触診で確認できる、特徴的な「羊皮紙の歯ごたえ」を伴う凝縮された焦点。
一般的に、症状は局所症状と全身症状に分けられます。局所症状は視覚的に確認され、特に骨片の湾曲や膨隆が確認できます。病変部位の皮膚の変化にも注意が必要です。血管のパターンが明瞭に現れ、組織は腫脹または扁平化します。腫瘍は触診で確認でき、多くの場合無痛ですが、特徴的な構造をしています。悪性腫瘍は典型的には塊状で不規則な形状をしています。
隣接する関節の動きが制限され、持続的な痛みが生じることがあります。血管や神経幹が圧迫されるため、感覚障害が起こりやすく、持続的な腫れが生じます。リンパ系も反応し、近くのリンパ節が腫れることがあります。
一般的な症状は悪性骨芽細胞腫に典型的であり、体内の中毒過程によるものです。患者には以下のような症状が現れることがあります。
- 発熱、発熱状態;
- やつれ;
- 継続的な弱さ。
- 眠気または不眠、食欲不振;
- 夜間の過度の発汗;
- 崩壊。
骨芽細胞腫も少数存在しますが、通常は小さく、臨床的には明らかではありません。他の理由により、放射線学的検査や画像検査中に偶然発見されることがあります。
骨芽細胞腫の骨化の最初の兆候
- 腫瘍の成長を加速させます。
- 疼痛症候群の増加。
- 破壊的な焦点の直径の拡大、または細胞小柱形態から溶解形態への変化。
- 比較的長い領域にわたる皮質層の崩壊。
- 破壊的な焦点の構成の明瞭性が失われます。
- 髄管を塞ぐために使用されていた閉鎖プレートの崩壊。
- 骨膜反応。
骨芽細胞腫の悪性度は、臨床的および放射線学的指標に基づいており、腫瘍組織の形態学的診断によって必ず確認されます。
当初は良性であった腫瘍の骨可塑化に加えて、原発性悪性骨芽細胞腫も存在します。実際、このような腫瘍は骨形成性肉腫の一種です。
悪性骨芽細胞腫の発生部位は良性骨芽細胞腫の場合と同じです。X線検査では、骨組織に明確な輪郭を示さない破壊巣が認められます。皮質層の破壊は広範囲に及び、しばしば軟部組織構造への進展が観察されます。
悪性骨芽細胞腫と骨芽性破骨肉腫を区別する兆候:
- 患者の大部分が高齢者であること
- 症状があまり鮮明でない;
- より良好な長期予後。
小児の骨芽細胞腫
小児期の骨芽細胞腫はまれで、100万人あたりわずか2~3例です。小児患者の大部分は10~15歳以上であることに留意する必要があります。
科学者たちは、小児における骨芽細胞腫の正確な原因を特定できていません。おそらく、この病理は小児の急激な成長と遺伝的要因に関連していると考えられます。
放射線被曝(特に放射線療法)、化学療法(細胞増殖抑制剤の服用)なども原因として挙げられます。多くの化学療法薬は骨細胞の遺伝物質を破壊し、腫瘍形成につながる可能性があります。
さらに、両眼性網膜芽細胞腫やリ・フラウメニ症候群などの特定の先天性疾患を持つ小児では、骨芽細胞腫のリスクが高くなります。また、パジェット病との因果関係も認められます。
また、大多数の子供(約 90%)では、医師が上記のリスク要因をまったく検出できないこともわかっています。
小児期の骨芽細胞腫の経過を予測することは困難であり、それは特定の腫瘍の特徴、腫瘍の局在、診断時の広がりの程度、治療の適時性、腫瘍の除去の完全性に依存するからです。
骨芽細胞腫の治療の質は、過去20~30年で大きく進歩しました。治療プロトコルは統合され、治癒率は70~80%以上に向上しました。腫瘍を根治的に切除し、十分な化学療法でその効果を増強できれば、良好な転帰が得られると言えます。良性の骨芽細胞腫を患う小児患者は、最も回復の見込みが高いと言えます。
治癒した患者の具体的な数字が発表されても、それはあくまでも一般的な数字であり、統計によって特定の子どもの回復の可能性を正確に予測・判断することはできません。「回復」とは、主に「体内の腫瘍の進行が消失した状態」と理解されています。現代の治療法は、長期的な再発の予防を可能にしているからです。しかし、望ましくない副作用や晩期合併症の可能性も忘れてはなりません。したがって、治療の複雑さに関わらず、どのような治療も質の高いリハビリテーションと連携させる必要があります。さらに、子どもたちは長期にわたり整形外科的ケアを必要とします。
フォーム
骨組織腫瘍の分類は非常に広範囲にわたります。主に細胞構造の変化、腫瘍形成過程の形態学的特徴に注目し、腫瘍は以下の2つのカテゴリーに分類されます。
- 骨形成(骨細胞に基づいて形成される)
- 新生骨芽細胞(血管や結合組織構造など、他の細胞タイプの影響を受けて骨に形成される)。
骨芽細胞腫は主に良性の腫瘍です。しかしながら、腫瘍の成長が著しく、骨組織の破壊と菲薄化を招き、外科的介入が必須となる場合もあります。一方、巨細胞性骨芽細胞腫は悪性腫瘍となることもあります。
臨床的、放射線学的パラメータおよび形態学的画像に応じて、骨芽細胞腫の 3 つの基本的な形態が区別されます。
- 細胞型は主に高齢者に見られ、ゆっくりとした発達が特徴です。診断では、腫瘍巣と健常骨領域を臨床的に区別することは不可能で、肥厚した塊状の腫脹が明らかになります。
- 嚢胞性腫瘍は、まず痛みを伴います。触診では「羊皮紙を砕いたような」感覚が認められます。視覚的には、滑らかな凸面を呈し、ドーム状の骨腫瘍が認められます。
- 溶菌型はまれな病理学的変異と考えられており、主に思春期に発見されます。腫瘍の進行は急速に進み、患者は触診時を含む疼痛に悩まされ始めます。
巨細胞腫は骨格のほぼすべての骨に形成される可能性がありますが、四肢、肋骨、脊椎の管状骨がやや多く影響を受けます。下顎の骨芽細胞腫は、上顎の2倍の頻度で発生します。触診では、軟化領域を伴う高密度の腫瘍が認められます。患者の最も一般的な訴えは、食べ物を噛むときに出血して不快感を引き起こす膨らみの存在です。問題が進行するにつれて、顎関節の機能障害が補完されます。管状骨の中で、腫瘍は大腿骨と脛骨によく影響を及ぼします。大腿骨の骨芽細胞腫は、主に中年に見られます。この病気は、対応する関節の機能障害を伴い、跛行が発生し、腫瘍の上の皮膚が顕著な血管パターンで覆われます。
上記の分類に加えて、病理学的には中枢型と末梢型がありますが、両者の間に形態学的差異はありません。末梢型骨芽細胞腫は歯肉に局在し、中枢型は骨に発生し、骨内に多発性出血を伴うことで区別されます(そのため、中枢型骨芽細胞腫の別名は褐色腫瘍です)。褐色に見えるのは、赤血球が沈着し、ヘモジデリンの形成とともに崩壊するためです。
悪性骨腫瘍は、以下のような段階を経て進行します。
- 3〜5 cm の T1 病巣が骨と 1 つの筋筋膜セグメント内にあります。
- T2 病巣は骨の経路に沿って 10 cm 以内に広がりますが、1 つの筋膜ケースを超えて広がることはありません。
- T3 病巣は 1 つの筋筋膜ケースの境界を離れ、近くのケースに広がります。
- T4 病巣は皮膚または神経血管幹から発生します。
同様に、リンパ節転移の程度や転移の広がりも分類されます。
合併症とその結果
骨芽細胞腫の合併症の一つとして、腫瘍の活動性亢進が挙げられます。これは特に、長期間の活動休止期間を背景に発生することが多く、このような症例では、腫瘍の悪性化、あるいは周囲の敏感な解剖学的構造への腫瘍の増殖が問題となります。
- 神経幹への転移は、大口径神経への影響により神経障害性疼痛症候群の発症を引き起こします。このような痛みは、従来の鎮痛剤を服用しても実質的に消失せず、患者を文字通り疲弊させます。
- 血管への転移は、突然の大量出血や血腫形成を伴う複雑な症状を引き起こす可能性があります。
合併症の可能性も否定できませんが、それには近くの関節の機能障害が伴います。このような状況で骨芽細胞腫が増殖すると、筋骨格機構の適切な機能が阻害され、可動域が制限され、疼痛症候群が発生します。
骨芽細胞腫の最も一般的な合併症は、患部における病的骨折と考えられています。骨組織が極めて脆く不安定になるため、軽微な外傷性衝撃でも問題が発生します。
さらに、専門家は悪性骨芽細胞腫に特徴的な特定の全身的および局所的な副作用についても話しています。
- 遠隔転移および近接転移の形成;
- 腐敗生成物による身体の中毒。
最初の診断措置からしばらく経ってから転移が検出された場合、継続中の治療が無効であり、腫瘍が進行していることを示します。
別の一連の合併症としては、骨芽細胞腫の骨病巣に対する化学療法や放射線照射による新たな腫瘍や全身病変の出現が挙げられます。
診断 骨芽細胞腫
骨芽細胞腫の検出に使用される診断方法には以下のものがあります。
- 臨床的検査には、病理学的に変化した領域の外部検査および触診が含まれます。
- X 線検査(前後方向および側面方向のレントゲン撮影、必要に応じて標的および斜め方向のレントゲン撮影)
- 断層撮影(コンピューター画像または磁気共鳴画像を使用)
- 放射性同位元素;
- 形態学的には、穿刺またはトレパノ生検中に得られた生体材料の組織学的、組織化学的、細胞学的分析が含まれます。
- 研究室。
医師は病歴を綿密に調査し、最初の兆候を特定し、疼痛症候群の部位と種類、その特徴を特定し、過去の検査結果と治療経過を考慮し、患者の全身状態の推移を評価します。長管骨の病変が疑われる場合、専門医は腫脹、近接関節の運動制限、神経症状、筋力低下、および低栄養の有無に注意を払います。内臓への転移の可能性がないか注意深く検査することが重要です。
すべての患者は、血液検査と尿検査を受け、タンパク質およびタンパク質分画、リン、カルシウム、シアル酸を測定します。また、ホスファターゼの酵素活性を測定し、デフィニル試験を実施し、C反応性タンパク質指数を調べる必要があります。骨芽細胞腫と骨髄腫の鑑別が必要な場合、病的なベンス・ジョーンズタンパク質の存在を確認する尿検査を実施します。
骨芽細胞腫の診断には、放射線学的診断が不可欠です。病変の位置、種類、他の組織や臓器への広がりを明らかにするために、定期的な検査と標的X線撮影、高画質の断層撮影が必須です。CT検査により、必要な平面における軟部組織や最も薄い骨構造の状態を明らかにし、病変の深部破壊巣を特定し、骨境界におけるそれらのパラメータを描写し、周囲組織の損傷度を決定することが可能です。
同時に、MRIは最も有益な診断法と考えられており、X線検査やCT検査に比べて多くの利点があります。この方法では、最も薄い組織層まで検査し、空間的な3次元画像を用いて病理学的変化を画像化することができます。
必須の器械診断は形態学的検査に代表されます。穿刺生検、穿頭生検、または腫瘍を含む骨片の切除時に採取された生体材料を評価します。穿刺生検は、特殊な針と放射線学的管理を用いて実施されます。
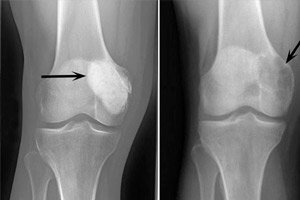
以下のX線所見は骨芽細胞腫の典型的な所見と考えられています。
- 多孔性制限;
- 薄い骨梁化型における骨溶解の均一性。
- 特異な「シャボン玉」の構造を持つ仮性嚢胞性透光体の存在。
この放射線学的所見は、一次性または二次性の反応性骨形成性骨膜症を伴わないことを示しています。皮質層の菲薄化と萎縮が認められます。
悪性骨芽細胞腫は、血管の集中的な新生により静脈うっ滞が増加します。血管の変化は、血管新生が豊富な腫瘍のような外観を呈します。
差動診断
骨芽細胞腫の診断は非常に困難な場合があります。年齢の異なる患者において、骨肉腫や骨嚢胞との鑑別診断において問題が生じます。統計によると、骨芽細胞腫が骨肉腫と誤診される症例は3%以上、骨嚢胞が骨芽細胞腫と誤診される症例は14%近くあります。
以下の表はこれらの病状の主な兆候をまとめたものです。
指標 |
骨芽細胞腫 |
骨形成性骨肉腫 |
骨嚢胞 |
最も多く発症する年齢 |
20~30歳 |
20歳から26歳 |
14歳未満のお子様 |
位置 |
骨幹端骨端部 |
骨幹端骨端部 |
中骨幹端領域 |
骨の再構成 |
重度の非対称の膨らみ。 |
小さな横方向の拡張 |
紡錘形の膨らみ。 |
破壊的な焦点の構成 |
輪郭ははっきりしている |
輪郭はぼやけていて、明瞭さがない |
輪郭ははっきりしている |
脊柱管の状態 |
閉鎖プレートで覆われている |
腫瘍との境界で開く |
変更はありません。 |
皮質層の状態 |
薄く、繊維状で、不連続。 |
薄くなって台無しになった |
薄くて平らな |
硬化現象 |
非定型 |
現在 |
非定型 |
骨膜反応 |
不在 |
「骨膜バイザー」のような形で存在する |
不在 |
骨端線の状態 |
板は薄く、波状です。 |
初期段階では骨端線の一部はそのまま残る |
変更はありません。 |
近くの骨片 |
変更はありません。 |
骨粗鬆症の兆候 |
変更はありません。 |
必須の注意には、患者の年齢、病状の持続期間、影響を受けた病巣の位置、表に示されているその他の既往歴情報などの指標が必要です。
骨芽細胞腫がこのような病理学的プロセスと混同される場合、次のような診断エラーが最もよく発生します。
- 動脈瘤嚢胞(長い管状骨の骨幹または骨幹端に局在する)
- 単軸型の線維性骨異形成症(主に小児期に発症し、骨の膨張を伴わずに骨の湾曲を伴う)。
- 副甲状腺機能亢進性骨異栄養症(病巣と健康な骨領域との境界が明確でなく、骨の隆起が明らかでない)
- 孤立性癌性骨転移(湾曲した「侵食された」輪郭を持つ破壊的な病巣を特徴とする)。
良性の骨芽細胞腫は常に悪性化する可能性があることを念頭に置くことが重要です。悪性化の原因はまだ正確には特定されていませんが、科学者たちは外傷やホルモンバランスの変化(例えば妊娠中)が悪性化の一因となっていると考えています。また、遠隔放射線治療を繰り返すことで悪性化が起こったという観察結果もあります。
骨化の症状:
- 腫瘍は急速に成長し始めます。
- 痛みは悪化しています。
- 破壊焦点のサイズが大きくなり、細胞小柱相が溶解相に移行します。
- 皮質層が壊れつつあります。
- 破壊的な焦点の輪郭は不明瞭になります。
- ロックプレートが壊れています。
- 骨膜反応があります。
原発性悪性腫瘍(骨芽細胞肉腫)と悪性骨芽細胞腫の鑑別においては、病変の持続期間と動態画像におけるX線画像の評価に特に注意が払われます。原発性悪性腫瘍のX線画像では、骨芽細胞腫に典型的な骨突出や骨橋は認められず、輪郭が不明瞭な硬化領域が認められます。しかし、悪性化においては、健常骨部分への障壁として機能していた閉鎖板の小さな領域がしばしば認められます。
連絡先
処理 骨芽細胞腫
骨芽細胞腫の患者にとって、唯一の適切な治療法は手術です。最も穏やかな介入は、腫瘍の進行初期段階で行われ、患部組織を切除し、さらに移植片で空洞を充填することです。移植片は、患者の別の健康な骨から採取します。この介入は最も好ましい方法で、外傷も少なく、場合によっては根治性も低くなります。腫瘍とともに患部骨片を切除する方が、より確実な方法と考えられており、腫瘍の再発の可能性を最小限に抑えることができます。
放置された大きな骨芽細胞腫の場合、特に悪性化しやすい、またはすでに悪性化している場合は、手足の部分的または完全な切断がしばしば考慮されます。
一般的に、骨芽細胞腫の外科的治療の戦略は、病巣の位置、広がり、および攻撃性に応じて選択されます。
腫瘍が長管骨に影響を及ぼす場合は、次のような外科的介入に注意することが推奨されます。
- 良性、遅延性、細胞構造を有する病巣、および骨端線端辺縁部における病巣に対しては、同種形成術または自家形成術による辺縁切除術を行う。金属スクリューで固定する。
- 細胞性骨芽細胞腫が骨径の中央まで広がった場合は、顆頭の3分の2、骨幹の一部、および関節面を切除します。欠損部は関節軟骨同種移植片で充填し、タイボルトとスクリューでしっかりと固定します。
- 骨幹端骨端線の全長にわたる腐朽や病的骨折の場合、関節切除を伴う分節切除や同種移植による欠損部の充填などの治療法が用いられます。骨端線はセメント固定ロッドで固定されます。
- 大腿骨近位部の病的骨折や骨芽細胞腫の悪性化の場合は、人工股関節全置換術が行われます。
- 膝関節部における骨端切除の場合、固定を伴う異種物質移植が用いられます。その後の放射線治療を確実に行うため、チタン製ステムを延長した全人工関節が好まれる場合が多くあります。
- 病変が脛骨遠位端にある場合は、骨形成術による足関節固定術を行い、切除します。距骨が侵されている場合は、伸展関節固定術を行い、距骨を切除します。
- 頸椎病変では、C1およびC2椎骨への前方アクセスが行われます。前外側アクセスが望ましいです。Th1 -Th2レベルでは、第 3 肋間腔への斜め胸骨切開による前方アクセスが使用されます (血管を慎重に下方に移動します)。腫瘍が 3~5 胸椎体に影響している場合は、第 3 肋骨を切除する前外側アクセスが行われます。肩甲骨は、筋肉を切断することなく後方に移動します。骨芽細胞腫がTh11とL2の間の胸腰椎領域に見つかった場合は、右側の胸腰椎切開術が選択されます。仙骨の上位 3 つの椎骨の前部へのアクセスはより困難です。血管幹と尿管の慎重なドレナージを伴う前外側後腹膜右側アクセスが推奨されます。
- 椎体がひどく破壊されている場合、または病変が胸椎および腰仙椎の弓部領域に広がっている場合、この場合には、脊椎の経椎弓根経椎弓根固定術が行われ、その後、破壊された椎骨がさらなる自己形成術で除去されます。
- 額骨および坐骨骨に良性の骨芽細胞腫が検出された場合、病変部は骨移植を行わずに健常組織内で切除されます。寛骨臼の底部および上部が侵されている場合は、切除に加え、欠損部を補うための骨移植を行い、スポンジオシス固定具を用いて固定します。
- 腸骨、胸骨、または坐骨が影響を受けている場合は、構造同種移植による同種骨形成術、移植骨接合、セメント系プラスチック挿入、人工空洞への人工骨頭の再配置が行われます。
- 仙骨と L2が影響を受けている場合は、病的に変化した下部仙骨片 (S2まで) の後方アクセス切除、経椎弓根固定、および骨移植を伴う後腹膜法による前側からの腫瘍の除去を含む 2 段階の介入が行われます。
それぞれの特定の状況において、医師は、治療結果を改善し、患者の正常な生活の質を確保するために最新の技術を適用する可能性を考慮しながら、最も適切な外科的介入方法を決定します。
防止
骨芽細胞腫には、特異的な予防法はありません。まず第一に、このような腫瘍の発生原因に関する研究が不十分であることが原因です。多くの専門家は、骨系への外傷の予防を主要な予防策として重視しています。しかし、外傷が骨腫瘍の形成に直接影響を与えるという証拠はなく、多くの場合、外傷は既存の腫瘍プロセスに注目を集めるだけで、病変の起源に明らかな意義はなく、同時に腫瘍の増殖に寄与する可能性があります。
骨芽細胞腫は、例えば他の腫瘍過程の治療を目的として、過去に電離放射線に曝露された骨に形成されることが多いことを忘れてはなりません。放射線誘発性腫瘍は通常、放射線曝露後3年以内に発生します。
非特異的な予防策としては次のようなものがあります。
- 悪い習慣の排除;
- 健康的なライフスタイルを送ること。
- 高品質で持続可能な栄養。
- 適度な定期的な身体活動。
- 怪我の予防、体内のあらゆる病理学的プロセスのタイムリーな治療、免疫の安定化。
予測
病的骨折は、骨組織の患部でしばしば発生します。この場合、良性腫瘍は根治的治療法が用いられれば良好な予後となりますが、再発や病巣の悪性化の可能性は排除されません。良性骨芽細胞腫は、病巣が活発な成長と顕著な骨破壊を特徴とする場合、予後不良となる可能性も否定できません。このような腫瘍は骨片全体を急速に破壊する可能性があり、病的骨折の発症と骨機能の重大な障害を伴います。このような患者は、骨組織欠損部の外科的置換に問題を抱えることが多く、骨折の治癒不良に関連する合併症を発症します。
悪性骨芽細胞腫のあらゆる変異型の平均5年生存率は、小児および成人ともに70%と、非常に良好と言えるでしょう。したがって、多くの場合、このような腫瘍はかなりの治癒率を達成していると結論付けることができます。もちろん、腫瘍の進行過程の種類、進行期、病変の程度、悪性度といった点も非常に重要です。
明らかに、最も大きな脅威となるのは悪性骨芽細胞腫です。この場合、早期発見、手術による腫瘍部位の特定が容易であること、化学予防薬および放射線療法に対する感受性が高い場合にのみ、良好な予後が得られると言えます。


