アレルギー反応の第一段階が発見され、予防の新たな可能性が開かれる
最後に見直したもの: 02.07.2025
 ">
">デューク大学NUS医学部の科学者たちは、ピーナッツ、魚介類、花粉、ダニなどのアレルゲンに接触した後に、一連の反応がどのように始まるのかを解明しました。この発見はNature Immunology誌に掲載され、重度のアレルギー反応を予防する薬の開発につながる可能性があります。
免疫細胞の一種である肥満細胞は、ピーナッツやダニなどの無害な物質を脅威と誤認し、その脅威に対して第一波の生理活性化学物質を放出することが知られています。皮膚の下、血管周囲、そして呼吸器系や消化管の内壁に存在する肥満細胞が、蓄えられた生理活性物質を同時に血中に放出すると、即座に全身性ショックを引き起こし、迅速な介入がなければ致命的となる可能性があります。
世界保健機関(WHO)によると、世界人口の10%以上が食物アレルギーに苦しんでいます。アレルギーの数が増えるにつれて、食物誘発性アナフィラキシーや喘息の発生率も増加しています。シンガポールでは、5人に1人の子供が喘息を患っており、食物アレルギーはすでにアナフィラキシーショックの主な原因となっています。
デューク大学とNUSの研究チームは、生理活性化学物質を含むマスト細胞顆粒の放出が、インフラマソームと呼ばれる細胞内多タンパク質複合体の2つの構成要素によって制御されていることを発見しました。これまで、これらのインフラマソームタンパク質は、免疫細胞内で自発的に集合し、感染が検知された際に免疫系の他の部位に警告を発する可溶性化学物質を分泌するだけであることが知られていました。
デューク大学病理学名誉教授で、デューク大学・NUS新興感染症プログラムに所属し、本研究を主導したソマン・アブラハム教授は次のように述べています。「インフラマソームの構成要素が、通常は細胞中心部に密集しているマスト細胞顆粒を細胞表面へと輸送し、そこから放出させるという、驚くほど重要な役割を果たしていることを発見しました。この予想外の発見は、マスト細胞によって引き起こされるアナフィラキシーショックの連鎖反応を予防するための、的確な介入ターゲットを与えてくれます。」
アブラハム教授と研究チームは、2種類のインフラマソームタンパク質(NLRP3またはASC)のいずれかを欠損したマウスを研究しました。これらのマウスはアレルゲンにさらされてもアナフィラキシーショックを起こさなかったのです。
しかし、肥満細胞内のNLRP3とASCタンパク質が集まって個々の細胞内顆粒に結合し、研究者が顆粒小体と呼ぶ複合体を形成したときにアナフィラキシーショックが観察され、顆粒が「線路に付着する」のと同じように肥満細胞内の細胞骨格によって形成された線路に沿って顆粒の移動が促進されました。
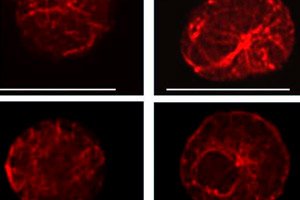
本論文の筆頭共著者であり、デューク大学・NUS新興感染症プログラムの主任研究員であるプラディープ・ビスト博士は、次のように述べています。「マスト細胞が活性化されると、微小管と呼ばれる動的な経路に沿って顆粒が細胞膜へと急速に移動し、そこから顆粒が直ちに細胞外へ放出される様子を観察しました。しかし、NLRP3またはASCタンパク質を欠損するマスト細胞では、顆粒の細胞内移動の証拠は見られず、顆粒は放出されませんでした。」
研究チームは、NLRP3 と ASC が顆粒輸送において果たす役割を実証した後、既知のインフラマソーム阻害剤に注目し、この現象を阻止できるかどうかを調べました。
慢性炎症性疾患の臨床試験で使用されているものと非常に類似したインフラマソーム阻害薬(CY-09)を用いて、マウスをアレルゲンに曝露させる前に投与しました。前臨床モデルにおいて、この薬剤によってアナフィラキシーショックを効果的に予防できることが分かりました。
上海交通大学医学部免疫療法研究所のアンドレア・メンカレッリ博士は、デューク大学シンガポール国立大学新興感染症プログラムに所属し、この論文の第一共著者である。同博士は次のように述べている。「驚くべきことに、インフラマソームタンパク質の活動を特異的に阻害する薬剤を使用することで、潜在的に有益な他の肥満細胞の機能に影響を与えることなく、予め蓄えられた肥満細胞の化学物質の放出を選択的に阻害することができました。」
これは根本的な治療法ではありませんが、重度のアレルギーを持つ人々にとって、潜在的に危険な反応の発生を防ぐ新たな手段となる可能性があります。現在、緊急治療は最初の症状が現れた直後に行われます。これらの治療は効果を発揮するためには限られた時間内に行う必要があり、深刻な副作用も伴います。
「重度の食物アレルギーを持つ子どもを持つ親にとって、曝露のリスクがないと確信できない状況に直面した際に、この薬が安心感を与えることは理解できます。免疫システムのこの部分を長期間にわたって不活性化することは望ましくありませんが、短期的な保護効果が得られる可能性はあります」とアブラハム教授は述べた。教授のチームは現在、アナフィラキシーショックに対する最良の保護効果を得るために、薬の投与量と使用頻度を最適化する研究を行っている。
「その後、喘息やアレルギー性皮膚反応についても同様のことをしたいと考えています。」
デューク大学NUS研究担当上級副学部長のパトリック・タン教授は、「この画期的な成果は、大きな応用の可能性を秘めており、さらなる研究だけでなく、重篤なアレルギー反応のリスクがある人々の生活の質の向上にもパラダイムシフトをもたらすものです。特に、常に不安を抱えながら暮らす幼い子どもを持つ親にとって、これは希望の光となるでしょう」と述べています。

