悪性卵巣腫瘍
記事の医療専門家
最後に見直したもの: 04.07.2025
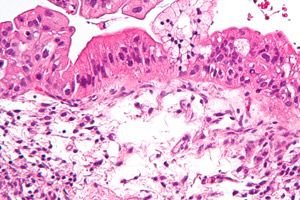
症状 卵巣悪性腫瘍
悪性卵巣腫瘍は、腹痛(引っ張られるような痛み、持続的な痛み、増加する痛み、突然の痛み、発作性の痛みなど)、全身状態の変化(疲労感、脱力感、口渇など)、体重減少、腹部の膨張、月経機能の変化、生殖管からの非周期的な血性分泌物の出現などの症状を特徴とします。
ステージ
現在、腫瘍学では悪性卵巣腫瘍のTNM分類を使用しています。
T – 原発性腫瘍。
- T0 – 原発腫瘍は検出されません。
- T1 – 腫瘍は卵巣に限られています。
- T1A – 腫瘍は片方の卵巣に限られており、腹水はありません。
- T1B – 腫瘍は両方の卵巣に限られ、腹水は発生しません。
- T1C - 腫瘍は片方または両方の卵巣に限られており、腹水または悪性細胞が腹部洗浄液中に存在します。
- T2 – 腫瘍が片方または両方の卵巣に影響を及ぼし、子宮傍組織にまで広がっています。
- T2A - 腫瘍が子宮および/または一方もしくは両方の卵管に拡大および/または転移しているが、臓側腹膜への浸潤および腹水は認められない。
- T2B – 腫瘍が他の組織に広がり、臓側腹膜に影響を及ぼすが、腹水は発生しない。
- T2C - 腫瘍が子宮および/または片方もしくは両方の卵管、および/または他の骨盤組織に広がっています。腹水。
- T3 - 腫瘍が片方または両方の卵巣に影響を及ぼし、小腸または大網に広がり、骨盤内に限局しているか、または骨盤外または後腹膜リンパ節に腹腔内転移があります。
N – 地域リンパ節。
- N0 – 所属リンパ節に損傷の兆候なし。
- N1 – 所属リンパ節に損傷がある。
- NX – 局所リンパ節の状態を評価するためのデータが不十分。
M – 遠隔転移。
- M0 – 遠隔転移の兆候なし。
- Ml – 遠隔転移があります。
- MX – 遠隔転移を判定するにはデータが不十分です。
実際には、卵巣がんの分類は、臨床検査と手術に基づいて決定される腫瘍の進行段階に応じて使用されます。
ステージI – 腫瘍が卵巣に限局している場合:
- ステージ 1a – 腫瘍は片方の卵巣に限られ、腹水はありません。
- ステージ16 – 腫瘍が両方の卵巣に限られている。
- ステージ 1b – 腫瘍は片方または両方の卵巣に限られていますが、明らかな腹水が見られたり、洗浄液中に異型細胞が検出されたりします。
ステージ II – 腫瘍が片方または両方の卵巣に影響を及ぼし、骨盤領域に広がります。
- ステージ IIa – 子宮および/または卵管の表面への広がりおよび/または転移;
- ステージ IIb – 腹膜や子宮を含む骨盤内の他の組織に転移している。
- ステージ IIb – IIa または II6 と同様に転移がみられるが、明らかな腹水がみられるか、洗浄液中に異型細胞が検出される。
ステージIII – 片側または両側の卵巣に転移し、骨盤外の腹膜転移および/または後腹膜リンパ節転移を伴う:
- ステージ IIIa – 腹膜内の顕微鏡的転移;
- ステージ IIIb – 腹膜内マクロ転移が 2 cm 以下
- ステージ IIIb – 2 cm を超える腹膜転移および/または局所リンパ節および大網転移。
ステージIV:片側または両側の卵巣に転移し、遠隔転移(遠隔リンパ節、肝臓、へそ、胸膜)を伴う。腹水。
診断 卵巣悪性腫瘍
患者の年齢は、さまざまな腫瘍の発生頻度、病気の進行、治療の予後を決定します。
患者の職業、特に好ましくない生産要因や環境要因にさらされる職業は、腫瘍の進行の危険因子となる可能性があります。
一般検査: 皮膚の色、体重減少、脚の腫れ、腹部の拡大、末梢リンパ節の状態、腹部の触診(大きさ、痛み、可動性、腫瘍の硬さ、腹水の存在)。
婦人科検査および膣直腸検査:子宮頸部および子宮体部の状態、付属器の腫瘍の存在、その大きさ、硬さ、周囲の臓器とのつながり、直腸膣中隔、ダグラス窩および子宮傍組織の状態。
追加の研究方法
骨盤内臓器の超音波検査、コンピューター断層撮影および磁気共鳴画像法、ダグラス窩の穿刺とそれに続く洗浄液の細胞学的検査、腫瘍の組織型を明らかにするための迅速生検および塗抹標本の採取を伴う診断的腹腔鏡検査(開腹手術)、および腹部臓器の修正(悪性腫瘍の場合は、腫瘍の広がりの程度を判定します)。
周囲臓器の状態や腫瘍の地形的特徴を明らかにするために、注腸鏡検査、排泄性尿路造影検査、線維性胃鏡検査、胸部臓器のX線検査などが適応となります。
卵巣癌の早期診断のための免疫学的方法 - 腫瘍マーカー CA-125 (漿液性および低分化腺癌の場合)、CA-119 (粘液性嚢胞腺癌および類内膜嚢胞腺癌の場合)、糖タンパク質ホルモン (顆粒膜細胞および粘液性卵巣癌の場合) の測定。
どのように調べる?
どのようなテストが必要ですか?
処理 卵巣悪性腫瘍
さまざまな卵巣腫瘍患者の治療の基本原則
良性腫瘍の場合 - 生殖年齢(45歳まで) - 患側の子宮付属器の切除。若年女性の両側性腫瘍の場合 - 卵巣組織の温存を前提とした腫瘍切除。閉経前後の場合 - 膣上切断術または子宮付属器を含む摘出。
悪性腫瘍 - ステージIおよびIIでは、治療は手術(子宮および付属器の摘出、大網の切除)から始まり、その後化学療法が行われます。ステージIIIおよびIVでは、多剤化学療法から始まり、その後細胞減量手術(腫瘍塊および転移巣の可能な限りの切除、膣上切断または子宮および付属器の摘出、大網および転移リンパ節の切除)が行われます。その後、多剤化学療法を繰り返します。
境界悪性腫瘍 - 子宮付属器切除術および大網切除術が適応となります。若年女性では、臓器温存手術(腫瘍摘出および大網切除)が可能であり、これに複数回の補助化学療法(特に腫瘍被膜浸潤または着床転移がある場合)を併用します。
現在、悪性卵巣腫瘍の患者に対する包括的な治療は、手術と多剤化学療法、および(または)骨盤および腹腔への遠隔放射線療法の組み合わせが適切であると考えられています。ほとんどの場合、手術から治療を開始することが望ましいです。腹水および胸水がある場合は、腹腔または胸腔内にプラチナ製剤を投与することができます。多剤化学療法には、作用機序の異なる複数の抗腫瘍薬が含まれます。術後には、摘出臓器の組織学的検査の結果を受けて、多剤化学療法が実施されます。
卵巣癌の多剤化学療法の標準レジメン
| スキーム | 作文、コース |
| SR | シスプラチン75 mg/ m2およびシクロホスファミド750 mg/ m2を3週間ごとに静脈内投与、6コース |
| 調査 | シスプラチン50 mg/ m2、ドキソルビシン50 mg/ m2、シクロホスファミド500 mg/m2を3週間ごとに静脈内投与し、6コース実施する。 |
| タキサン | パクリタキセル – 135 mg/m2 / 24時間、シスプラチン75 mg/ m2を3週間ごとに静脈内投与、6コース |
ほとんどの薬剤には、骨髄造血の抑制、白血球減少症、血小板減少症の発現に関連する副作用があり、その重症度は治療開始後2週間以内に最も高くなります。そのため、血球数をモニタリングし、白血球数が3 x 10 6 /L未満、血小板数が1 x 10 6 /L未満になった場合は抗腫瘍薬による治療を中止する必要があります。
薬剤に対する患者の耐性と、使用中に生じる反応の重症度も非常に重要です。特に、シクロホスファミドの使用は、吐き気、嘔吐、脱毛症、場合によっては筋肉痛や骨痛、頭痛、そしてまれに中毒性肝炎や膀胱炎を引き起こすことがあります。
化学療法の段階では、疾患の完全な退縮(すべての病状の消失、CA-125値の正常化)を目指し、その後2~3回の追加治療を実施して効果を強化する必要があります。部分的な退縮が達成された後、化学療法は、最後の2回の治療中に残存腫瘍の大きさと腫瘍マーカー値によって評価される、プロセスの安定化が認められるまで継続する必要があります。このような場合、ほとんどの患者で治療コース数は6~12回ですが、6回未満になることはありません。
化学療法薬の投与量を決定するには、体表面積(m²)を計算します。平均すると、身長160cm、体重60kgの場合、体表面積は1.6m² 、身長170cm、体重70kgの場合、体表面積は1.7m²となります。
現在、放射線療法は卵巣腫瘍患者の独立した治療法ではなく、術後期における併用療法の一つとして推奨されています。術後放射線療法は、臨床病期IおよびIIの患者、ならびに腹腔内の腫瘍塊の容積を減少させる腫瘍減量手術後の病期IIIの患者に適応となります。多くの場合、腹腔内への遠隔ガンマ線照射は22.5~25グレイの線量で行われ、小骨盤への追加照射(最大45グレイ)が行われます。これらの段階では、術後放射線療法に加えて2~3年間の「予防的」化学療法が行われます。臨床病期IVの悪性卵巣腫瘍患者に対する放射線療法は未解決の問題であり、大きな腫瘍塊および(または)漿液腔内の滲出液の存在は放射線療法の禁忌とみなされています。このような患者では、手術以外の追加治療法の選択は化学療法を優先すべきです。
国際産科婦人科学会(RGO)によれば、卵巣がんのすべてのステージにおける5年生存率は30〜35%を超えず、ステージIでは5年生存率は60〜70%、ステージIIでは40〜50%、ステージIIIでは10〜15%、ステージIVでは2〜7%です。
医薬品



 [
[