骨髄形成不全
記事の医療専門家
最後に見直したもの: 04.07.2025
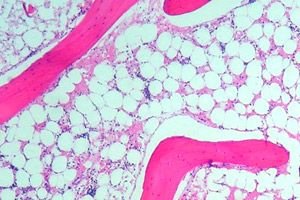
危険因子
骨髄形成不全の危険因子には以下のようなものがあります。
- 化合物:細胞増殖抑制薬 - 細胞分裂を阻害し、通常は腫瘍の治療に用いられます。一定量の薬剤を投与すると骨髄に損傷を与え、血球の形成を阻害する可能性があります。免疫抑制薬 - 体の免疫系を抑制し、免疫系が過剰に活性化し、自身の健康な組織に損傷を与えている場合に用いられます。服用を中止すると、造血機能が回復することがよくあります。
- 患者が特定の過敏症を有する場合、身体に影響を与える物質。抗生物質(抗菌薬)、ガソリン、水銀、様々な染料、クロラムフェニコール、金製剤などがこれに該当します。これらの物質は、骨髄機能の可逆的および不可逆的な破壊を引き起こす可能性があります。これらの物質は、皮膚、エアロゾルの吸入、経口(水や食物を含む)を通じて体内に侵入する可能性があります。
- イオン粒子(放射線)による照射 - 例えば、原子力発電所や放射線治療を用いて腫瘍を治療する医療機関で安全規則に違反した場合など。
- ウイルス感染症 - インフルエンザ、肝炎ウイルスなど
病因
骨髄無形成症の病因はまだ十分に研究されていません。現在、その発症メカニズムについてはいくつかの異なる説が考えられています。
- 骨髄は多能性幹細胞を通じて影響を受けます。
- 体液性または細胞性の免疫機構の影響により造血プロセスが抑制されます。
- 微小環境の構成要素が正しく機能しなくなる。
- 造血プロセスを促進する因子の欠乏の発症。
- 遺伝性骨髄不全症候群を引き起こす遺伝子の変異。
この病気では、造血に直接関わる成分(ビタミンB12、鉄、プロトポルフィリン)の含有量は減少しませんが、同時に、造血組織がそれらを利用できなくなります。
症状 骨髄形成不全
骨髄形成不全は、血液のどの細胞要素が影響を受けたかに応じて現れます。
- 赤血球数が減少すると、息切れ、全身倦怠感などの貧血の症状が現れます。
- 白血球のレベルが減少すると発熱が起こり、体の感染症に対する感受性が高まります。
- 血小板レベルが減少すると、出血症候群、点状出血、出血が発生する傾向があります。
骨髄の部分的赤血球無形成症では、赤血球産生の急激な減少、深部網状赤血球減少症、および孤立性の正色素性貧血が観察されます。
この疾患には先天性と後天性があります。後天性は、後天性の原発性赤芽球癆、あるいは他の疾患(肺がん、肝炎、白血病、伝染性単核球症、肺炎、鎌状赤血球貧血、おたふく風邪、潰瘍性大腸炎など)に伴って発症する症候群として現れます。
合併症とその結果
骨髄形成不全の合併症には以下のものがあります。
- 貧血性昏睡は、意識を失い、昏睡状態に陥る状態です。必要な量の酸素が脳に供給されないため、いかなる外部刺激にも反応しません。これは、血液中の赤血球数が急激かつ著しく減少するという事実によって起こります。
- 様々な出血(出血性合併症)が始まります。この場合の最悪の選択肢は出血性脳卒中(脳の一部が血液で浸潤し、その結果脳が壊死する)です。
- 感染症 – 微生物(さまざまな真菌、細菌、ウイルス)が感染症を引き起こします。
- 一部の内臓(腎臓や心臓など)の機能障害、特に慢性病理が併発している場合。
診断 骨髄形成不全
骨髄形成不全症を診断する際は、患者の病歴と訴え、つまり病気の症状がどのくらい前に現れたか、患者が症状の出現を何と関連付けているかが調査されます。
次に、患者の生涯履歴を明らかにします。
- 患者に併発する慢性疾患が存在する。
- 遺伝性疾患の存在。
- 患者さんには何か悪い習慣がありますか?
- 最近、長期間にわたり何らかの薬を服用したかどうかが明らかにされます。
- 患者の体内に腫瘍が存在すること。
- さまざまな有毒物質との接触はありましたか?
- 患者は放射線またはその他の放射線要因に曝露されましたか?
その後、身体検査が行われます。皮膚の色(骨髄形成不全症では蒼白が観察されます)、脈拍数(多くの場合速い)、血圧(低い)を測定します。粘膜と皮膚を検査し、出血や膿性小胞の有無などを確認します。
テスト
病気の診断の過程では、いくつかの臨床検査も行われます。
血液検査を実施します。骨髄無形成症の場合、ヘモグロビン値と赤血球数の減少が認められます。血液の色指数は正常範囲です。白血球を含む血小板数は減少し、さらに顆粒球含量の減少により白血球の適正な比率も崩れます。
尿検査も行われ、尿中に赤血球が存在するかどうか(これは出血症候群の兆候です)、または白血球と微生物が存在するかどうか(これは体内で感染性合併症が発生している兆候です)を判断します。
生化学血液検査も実施されます。血糖値、コレステロール値、尿酸値(臓器への同時損傷の有無を確認するため)、クレアチニン値、電解質(ナトリウム、カリウム、カルシウム)を測定します。
 [ 38 ], [ 39 ], [ 40 ], [ 41 ], [ 42 ], [ 43 ], [ 44 ]
[ 38 ], [ 39 ], [ 40 ], [ 41 ], [ 42 ], [ 43 ], [ 44 ]
機器診断
機器診断中は次の手順が実行されます。
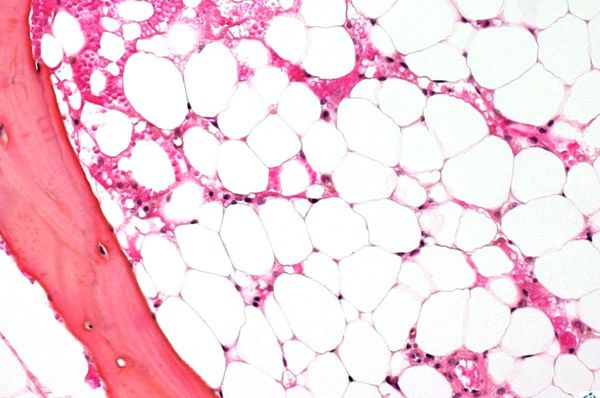
骨髄を検査するために、通常は胸骨または寛骨に穿刺(内部の内容物を採取する穿刺)を行います。顕微鏡検査によって、造血組織が瘢痕または脂肪に置き換わっているかどうかを判定します。
骨髄と周辺組織との関係を調べるトレフィン生検。この検査では、トレフィンと呼ばれる特殊な器具を使用し、腸骨から骨膜と骨とともに骨髄の柱を採取します。
心電図検査により、心筋の栄養と心臓のリズムに関する問題を特定できます。
どのようなテストが必要ですか?
連絡先
処理 骨髄形成不全
病因療法(原因に作用する)によって疾患を根絶することはほぼ不可能です。誘発因子の除去(例えば、投薬の中止、放射線照射区域からの離脱など)は有効ですが、この場合、骨髄細胞死の速度は低下するだけで、安定した造血機能を回復することはできません。
移植が不可能な場合(患者に適したドナーがいないなど)は、免疫抑制療法が用いられます。この場合、シクロスポリンA群または抗リンパ球グロブリン群の薬剤が使用されます。これらの薬剤を併用する場合もあります。
GM-CSF(白血球の産生を刺激する薬剤)の使用。白血球数が2×109 g/L未満に低下した場合、この治療が行われます。この場合、コルチコステロイド薬も使用されることがあります。
タンパク質の形成を刺激するアナボリックステロイドが使用されます。
骨髄形成不全症の治療には以下の方法が使用されます。
- 血液成分の輸血。
輸血は洗浄赤血球(タンパク質を除去したドナーの赤血球)を用いて行われます。この方法により、輸血に伴う副作用の重症度と頻度を軽減できます。このような輸血は、患者の生命が脅かされる場合にのみ行われます。具体的には、以下の状況が挙げられます。
- 患者が貧血性昏睡に陥る。
- 重度の貧血(この場合、ヘモグロビン値が 70 g/l を下回ります)。
患者が出血を経験し、血小板数が明らかに減少している場合は、ドナー血小板の輸血が行われます。
止血療法は出血が始まった部位に応じて行われます。
感染性合併症が発生した場合、以下の治療法が用いられます。
- 抗菌治療。これは、鼻咽頭スワブ、尿培養、血液培養を採取し、感染の原因となった微生物を特定し、抗生物質に対する感受性を判定した後に行われます。
- 全身抗真菌治療は必須です。
- 感染の入り口となる可能性のある部位(細菌、真菌、またはウイルスが体内に侵入する場所)に対する局所消毒療法。このような処置では通常、異なる薬剤を順番に使用しながら口をすすぐことが含まれます。
薬
骨髄無形成症の場合、薬物療法が必須です。最も一般的に使用される薬剤は、細胞増殖抑制薬(6-メルカプトプリル、シクロホスファミド、メトトレキサート、シクロスポリンA、イムラン)、免疫抑制薬(デキサメタゾン、メチルプレドニゾロン)、抗生物質(マクロライド系、セファロスポリン系、クロロキノロン系、アザライド系)の3つの薬剤群です。腸内細菌叢の異常や血圧の異常を改善する薬剤、酵素薬などが使用される場合もあります。
メチルプレドニゾロンは経口投与されます。臓器移植の場合は、1日0.007g以下の用量で投与されます。
薬の副作用:体内に水分とナトリウムが保持される、血圧が上昇する、カリウムが失われる、骨粗鬆症、筋力低下、薬剤性胃炎、さまざまな感染症に対する抵抗力が低下する、副腎活動の抑制、一部の精神障害、月経周期の問題。
この薬は、重度の高血圧、第3段階の循環不全、妊娠、急性心内膜炎、腎炎、さまざまな精神病、骨粗鬆症、十二指腸または胃の潰瘍、最近の手術後、結核や梅毒の活動期、高齢者、12歳未満の子供には禁忌です。
メチルプレドニゾロンは、糖尿病患者には、絶対的な適応がある場合、または抗インスリン抗体価の高いインスリン抵抗性患者の治療にのみ、慎重に処方されます。結核または感染症の場合、この薬剤は抗生物質または結核治療薬との併用でのみ使用できます。
イムラン - 初日は、体重1kgあたり1日5mg以下の用量で使用できます(2~3回に分けて服用する必要があります)。ただし、投与量は通常、免疫抑制療法によって異なります。維持用量は、体重1kgあたり1日1~4mgです。これは、患者の体への耐性と臨床状態に応じて決定されます。研究によると、イムランによる治療は、少量からでも長期間にわたって実施する必要があることが示されています。
過剰摂取は、喉の潰瘍、出血、あざ、感染症を引き起こす可能性があります。これらの症状は、慢性的な過剰摂取でより多く見られます。
副作用 - 骨髄移植後、アザチオプリンを他の免疫抑制剤と併用して治療を受けた患者は、細菌、真菌、またはウイルスによる感染症を経験することがよくあります。その他の副作用としては、不整脈、髄膜炎の兆候、頭痛、唇や口腔の病変、知覚異常などがあります。
シクロスポリンAは静脈内投与されます。1日量を2回に分けて、2~6時間前に投与します。初回投与量は3~5mg/kgで十分です。骨髄移植を受けた患者の治療には、静脈内投与が最適です。移植前(手術の4~12時間前)に10~15mg/kgを経口投与し、その後1~2週間は同じ用量を投与します。その後、通常の維持用量(約2~6mg/kg)まで減量します。
過剰摂取の症状には、眠気、激しい嘔吐、頻脈、頭痛、重度の腎不全の発症などがあります。
シクロスポリンを服用する際は、以下の注意事項を守ってください。治療は、免疫抑制剤を用いた患者の治療に豊富な経験を持つ医師によって、病院で実施される必要があります。シクロスポリンの服用により、悪性リンパ増殖性腫瘍を発症するリスクが高まることを覚えておく必要があります。そのため、服用を開始する前に、治療の効果が関連するすべてのリスクに見合うかどうかを判断する必要があります。妊娠中は、厳格な適応症がある場合のみ、この薬の使用が許可されます。静脈内投与によりアナフィラキシー様反応のリスクがあるため、予防のために抗ヒスタミン薬を服用し、患者はできるだけ早く経口投与に移行する必要があります。
ビタミン
患者に出血がある場合は、血液療法に加えて、10%塩化カルシウム溶液(経口)とビタミンK(1日15~20mg)を服用する必要があります。さらに、アスコルビン酸(0.5~1g /日)とビタミンP(0.15~0.3g /日の用量)を大量に処方します。葉酸(最大200mg /日)とビタミンB6(できれば注射剤(ピリドキシン50mg /日))を服用することが推奨されます。
理学療法治療
骨髄を活性化するために、理学療法、すなわち脛または胸骨領域の管状骨へのジアテルミー療法が用いられます。この処置は毎日20分間行う必要があります。ただし、この方法は顕著な出血がない場合に限り可能です。
外科的治療
重度形成不全症の場合、骨髄移植が行われます。患者が若く、ドナーからの血液成分の輸血回数が少ない場合(10回以下)は、この手術の有効性が向上します。
この治療法では、ドナーから骨髄を採取し、それをレシピエントに移植します。幹細胞懸濁液を移植する前に、細胞増殖抑制剤で処理します。
移植後、患者は長期間の免疫抑制治療を受けることになりますが、これは移植片の拒絶反応やその他の免疫反応を防ぐために必要です。
骨髄無形成症の研究に関連する権威ある書籍と研究のリスト
- 書籍:「再生不良性貧血:病態生理と治療」著者:Hubert Schrezenmeier、Andrea Bacigalupo発行年:2009
- 書籍:「再生不良性貧血およびその他の骨髄不全症候群」著者:ニール・S・ヤング、コリン・G・スチュワード発行年:2018年
- 研究:「小児における後天性再生不良性貧血の診断と管理」著者:モニカ・ベスラー、ブランシュ・P・アルター年:2016年
- 研究:「再生不良性貧血:病因、診断、および管理」著者: Jaroslaw P. Maciejewski、Neal S. Young年: 2018
- 書籍:「再生不良性貧血」著者:ジョン・W・アダムソン出版年:2009


